Spannungsquellen
Inhalt
Nicht aufladbare Spannungsquellen
Batterie
Eine Batterie ist eine Spannungsquelle, die nur einmal vollständig entladen werden kann. Vielfach steht auf der Batterie, welche Spannung sie im Neuzustand hat. Diese wird in der Einheit Volt (V) angegeben.
Apfelbatterie

Apfelbatterie
Stecke zwei Platten oder Stifte aus verschiedenen Metallen (z. B. Zink und Kupfer) in einen Apfel oder eine Orange. Schließe ein Voltmeter an. Wähle einen Messbereich von wenigen Volt aus.
Gib an, welche Spannung du ablesen kannst.
Du bist nicht angemeldet.
Registriere dich oder melde dich an, um deinen Text zu dieser Aufgabe zu speichern.
Wiederhole das Experiment mit zwei gleichen Metallplatten oder Metallstiften.
Gib an, welche Spannung du ablesen kannst.
Du bist nicht angemeldet.
Registriere dich oder melde dich an, um deinen Text zu dieser Aufgabe zu speichern.
Woher kommt die Spannung?
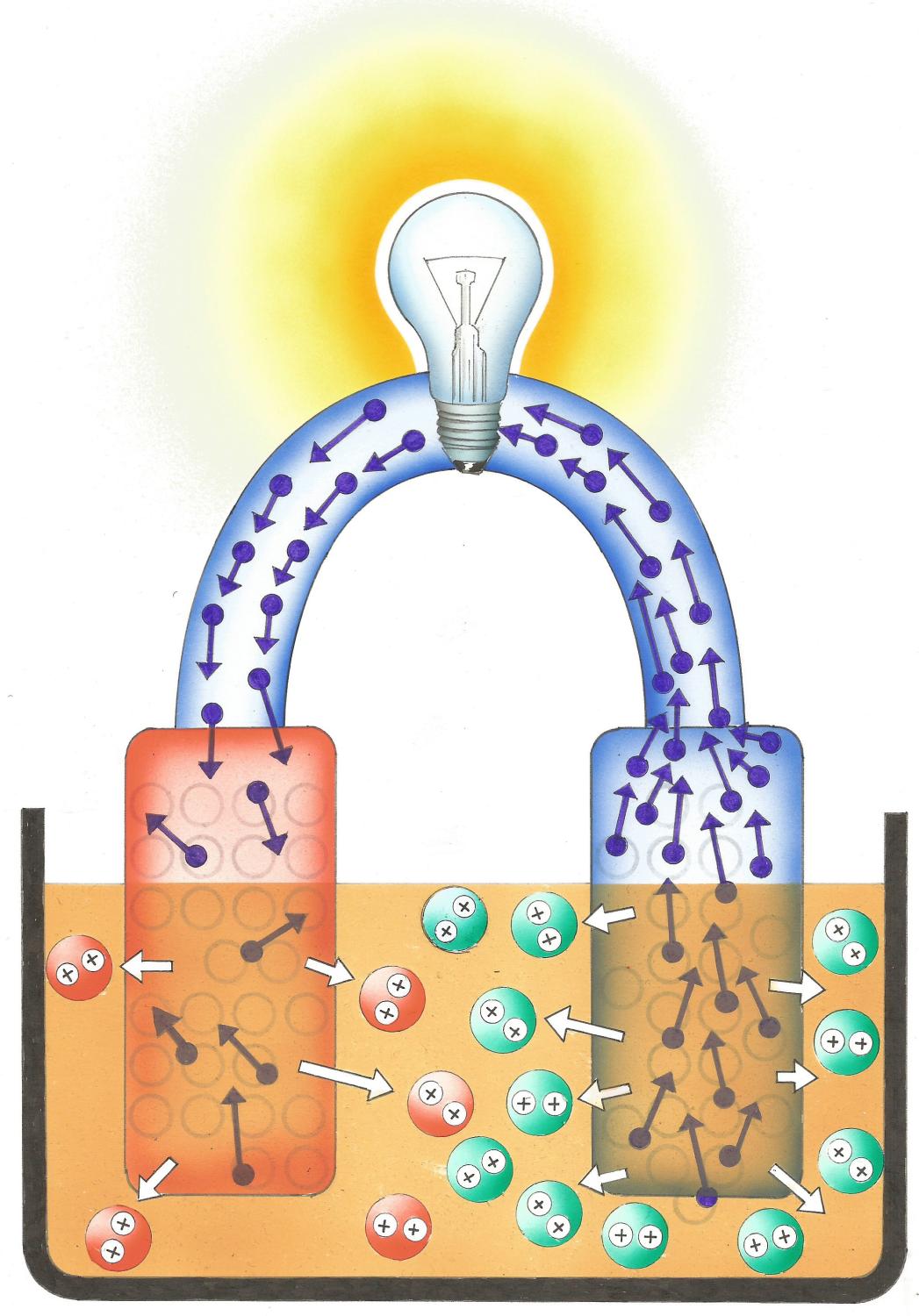
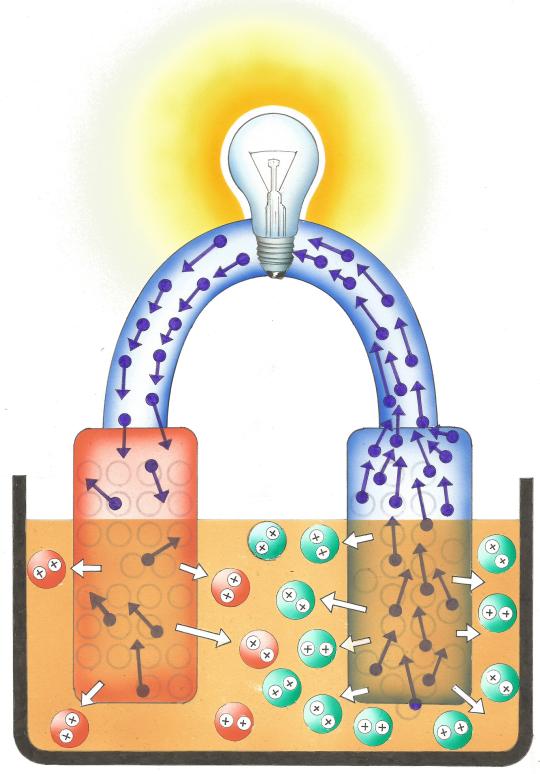
Die Metallplatten werden von der Säure des Apfels bzw. der Orange angegriffen. Aus der Oberfläche des Obstes werden positive Ionen herausgelöst, sodass sich die Metallplatten negativ aufladen, allerdings unterschiedlich stark. Zwischen den beiden Platten besteht ein Ladungsunterschied, eine elektrische Spannung.
Verbindet man die beiden Metallplatten, so bewegen sich Elektronen von der Platte mit mehr Elektronen zur anderen. Es fließt ein Strom.
Voltaelement
Eine Kupfer- und eine Zinkplatte in verdünnter Schwefelsäure stellen ein Voltaelement dar. Es liefert eine Spannung von ziemlich genau 1 Volt. Die Flüssigkeit, die den Ladungstransport ermöglicht, nennt man Elektrolyt.
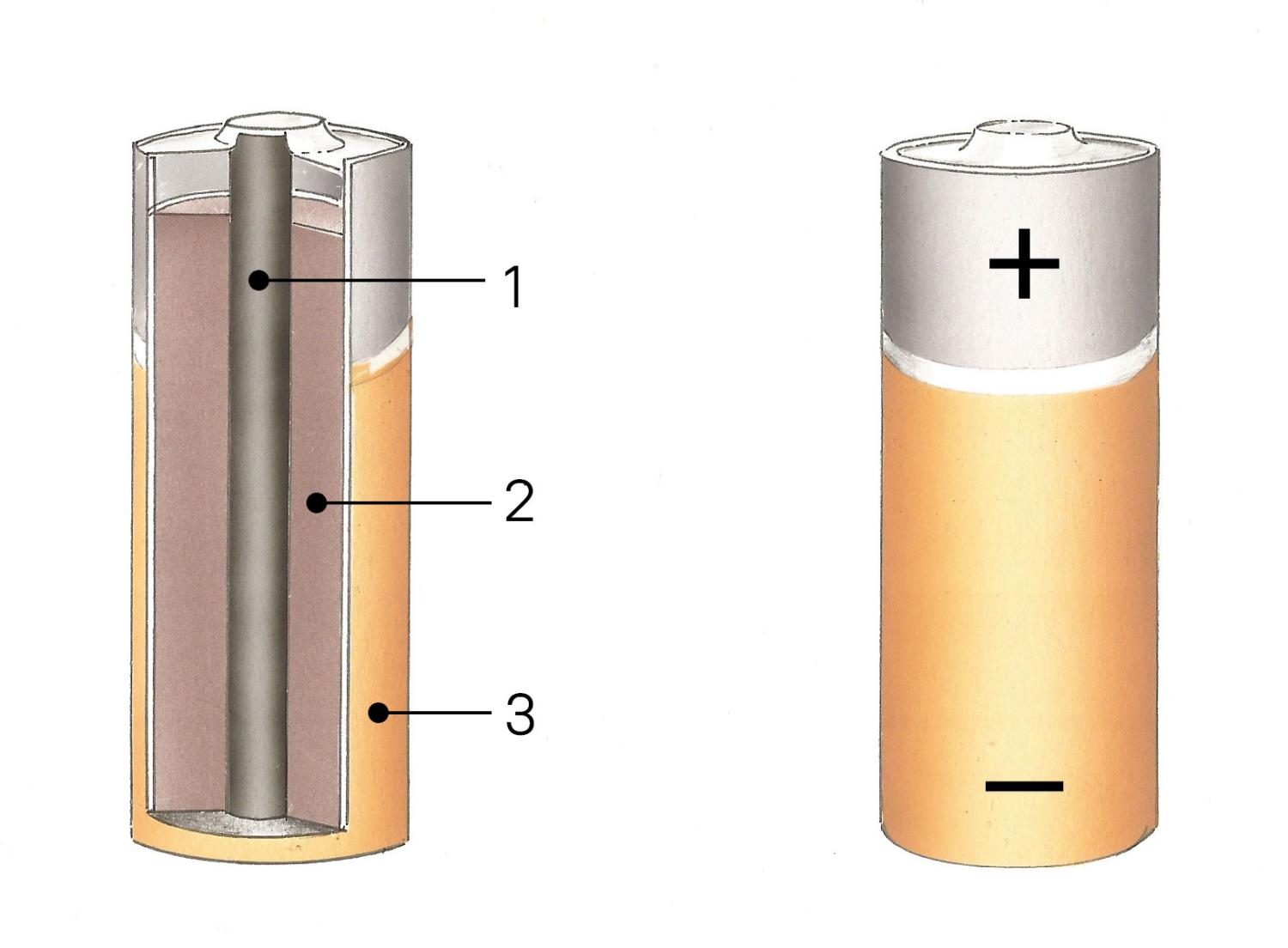
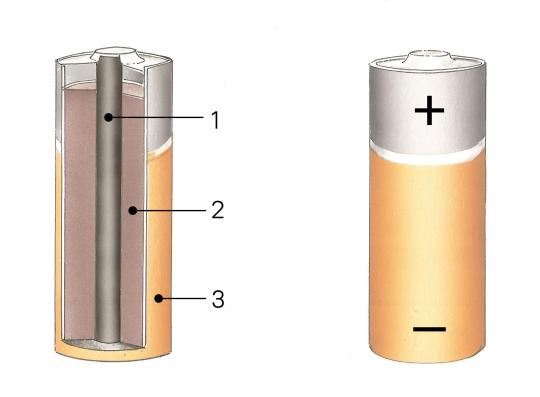
Eine häufig verwendete und billige Batterie ist das Trockenelement. Dabei bildet ein Zinkbecher (3) den negativen Pol. Salmiakpaste mit Braunstein (2) umhüllt als Elektrolyt einen Kohlestab (1), der den positiven Pol bildet. Eine solche Batterie liefert 1,5 V.
Knopfzellen und Entsorgung von Batterien
Knopfzellen sind runde, sehr flache Batterien mit einer Spannung zwischen 1,35 und 3,6 Volt. Beim Großteil der Knopfzellen wird der positive Pol von Quecksilberoxid gebildet, der negative Pol von Zink.
Knopfzellen werden als Spannungsquelle in Geräten eingesetzt, die einen geringen Strombedarf haben und klein sind, z. B. in Taschenrechnern, Armbanduhren und Hörgeräten.
Verbrauchte Batterien gehören zum Sondermüll. Sie enthalten Stoffe, wie z. B. Quecksilber, die die Umwelt gefährden. Beim Kauf einer neuen Batterie muss die alte zurückgenommen und dann entsprechend entsorgt werden

Aufladbare Spannungsquellen
Akkumulatoren
Ein Akkumulator ist eine Batterie, die mehrmals wieder aufgeladen werden kann. Beim Aufladen wird durch chemische Prozesse der Ladungsunterschied zwischen den Anschlüssen wiederhergestellt.

Die Stromquellen von Autos sind meist Bleiakkumulatoren. Dabei tauchen zwei Bleiplatten in verdünnte Schwefelsäure ein. Durch das Aufladen mit elektrischem Strom werden die Oberflächen der beiden Platten chemisch verändert und es kann damit elektrische Energie gespeichert werden. Die Spannung an den Polen einer Bleizelle beträgt etwa 2 Volt. Bei einer Autobatterie sind meist 6 Zellen zusammengeschaltet, sodass der Akkumulator eine Spannung von 12 V hat. Die Energie des Akkumulators in einem Auto wird durch die Arbeit des Motors laufend nachgeliefert.
Beim Laden des Bleiakkumulators wird elektrische Energie in chemische Energie umgewandelt. Die Oberflächen der beiden Bleiplatten verändern sich unterschiedlich. Bei einem aufgeladenen Bleiakkumulator besteht zwischen den beiden Bleiplatten mit unterschiedlichen Oberflächen ein Ladungsunterschied.
Beim Entladen wird chemische Energie wieder in elektrische Energie umgewandelt. Der Ladungsunterschied wird schwächer und verschwindet schließlich.

Lithium-Ionen-Akkumulatoren können viel Energie speichern, erfordern jedoch in den meisten Anwendungen elektronische Schutzschaltungen, da sie sowohl auf komplette Entladung als auch auf Überladung empfindlich reagieren. Die Materialien in der negativen und in der positiven Elektrode sowie der Elektrolyt enthalten Lithiumionen.
Lithium-Ionen-Akkus versorgten anfangs hauptsächlich tragbare Geräte mit hohem Energiebedarf, beispielsweise Mobiltelefone, Tablets, Digitalkameras, Camcorder, Notebooks. Lithium-Ionen-Akkus sollten einer Wiederverwertung zugeführt werden, damit der wertvolle Rohstoff nicht verloren geht.
Verschiedene Arten von Lithium-Akkus werden auch für Elektroautos verwendet.

Training
Setze die richtigen Wörter aus der Liste in die Lücken ein.
Ladungsunterschied – Oberflächen – stärker – Bleiplatten – Laden – chemische – elektrische – schwächer
| Beim |
| eines Bleiakkumulators wird |
| Energie in chemische Energie umgewandelt. |
| Die |
| der beiden Bleiplatten verändern sich unterschiedlich. |
| Bei einem aufgeladenen Bleiakkumulator besteht zwischen den beiden |
| ein |
| . |
| Beim Entladen wird |
| Energie wieder in elektrische Energie umgewandelt. |
| Der Ladungsunterschied wird |
| und verschwindet schließlich. |
Richtig oder falsch?
Markiere das Zutreffende.
| richtig | falsch | |
|---|---|---|
| Die Säure löst Protonen aus der Zinkplatte. (K / N) | ||
| Die Säure löst positive Ionen aus der Zinkplatte. (T / S) | ||
| Auf den Platten in der Säure bildet sich ein Überschuss an Elektronen. (G / H) | ||
| Alle Metallplatten laden sich in der Säure gleich stark auf. (U / V) | ||
| Zwischen verschiedenen Metallplatten in einer Säure bildet sich eine Spannung. (E / D) | ||
| Auf der Kupferplatte in der Säure sind weniger Elektronen als auf der Zinkplatte. (I / L) | ||
| Die Spannung eines Voltaelements beträgt 12 V. (B / A) |
Die Buchstaben der richtigen Antworten ergeben in der richtigen Reihenfolge das Lösungswort:

Beschrifte die Teile der Zink-Kohle-Batterie.
| 1 | |
| 2 | |
| 3 |
Gestalte mit deiner Sitznachbarin/deinem Sitznachbarn ein Quiz zum Thema „Aufladbare Spannungsquellen”.
Formuliere zwei W-Fragen, zwei Multiple-Choice-Aufgaben und drei im Format richtig/falsch.
Tauscht eure Aufgaben in der Klasse aus.
Du bist nicht angemeldet.
Registriere dich oder melde dich an, um deinen Text zu dieser Aufgabe zu speichern.

Nimm in die linke Hand eine Kupferplatte, in die rechte Hand eine Zinkplatte und schließe die Platten an ein Voltmeter an.
Halte die Platten mit der ganzen Hand, dann mit den Fingerspitzen. Greife dann zum Vergleich die Platten mit nassen Händen an.
Gib jeweils die Spannung an:
Wann war die Spannung am größten?
Mensch als Batterie
Die Feuchtigkeit der Hände wirkt wie die Säure der Orange bei der Orangenbatterie. Deshalb kann man eine Spannung zwischen den beiden Metallplatten nachweisen.
Luigi Galvani und die Froschschenkel
Luigi Galvani war Professor der Anatomie an der Universität Bologna. Man dachte damals, dass die Nerven von Lebewesen eine geheimnisvolle Elektrizität enthielten. Diese würde die Wahrnehmung der Sinne und die Steuerung der Muskeln ermöglichen.
Galvani war auf der Suche nach dieser Elektrizität. Er experimentierte mit Froschschenkeln. Diese hängte er mit Messinghaken an einem Eisengitter auf. Wenn die Froschschenkel durch einen Windstoß gegen das Gitter schlugen, zuckten die Muskeln.
Galvani glaubte, eine geheimnisvolle Lebenskraft entdeckt zu haben.
In Wirklichkeit hatte er etwas Ähnliches wie eine Batterie vor sich, zwei Metalle und einen Elektrolyten, das Wasser im Gewebe der Froschschenkel.

Lies den Text durch.
Begründe, weshalb es sich um eine Art Batterie handelt.
Du bist nicht angemeldet.
Registriere dich oder melde dich an, um deinen Text zu dieser Aufgabe zu speichern.
Formuliere dann Fragen zum Text und stelle sie deinen Mitschülerinnen und Mitschülern.
Du bist nicht angemeldet.
Registriere dich oder melde dich an, um deinen Text zu dieser Aufgabe zu speichern.
Schreibe die Geschichte auf, wie Luigi Galvani sie erzählt haben könnte.
Du bist nicht angemeldet.
Registriere dich oder melde dich an, um deinen Text zu dieser Aufgabe zu speichern.
Suche nach Informationen zu Luigi Galvani.
Recherchiere im Internet!
Schreibe einen kurzen Lebenslauf von ihm.
Du bist nicht angemeldet.
Registriere dich oder melde dich an, um deinen Text zu dieser Aufgabe zu speichern.
Merke
Batterien und Akkumulatoren sind Spannungsquellen, die chemische Energie in elektrische Energie umwandeln.
Batterien können nicht wieder aufgeladen werden, Akkumulatoren schon.